Toxoplasma gondii
Aspect
- Phylum: Apicomplexa
- Ordre: eucoccidiorida
- Espèce: toxoplasmosa gondii
- C’est un parasite intracellulaire

Pathogenese
Il existe 2 formes de base: kystes avec les bradyzoites (dans les tissus de l’hôte intermédiaire) et oocystes avec sporozoites (excrété par les chats)
- Cycle dixène avec 2 hôtes vertébrés et des phases de multiplication sexuée et asexuée.
Hôte définitf: chat qui après avoir ingéré l’hôte intermédiaire sera contaminé par les kystes (avec bradyzoites à l’intérieur) qui vont suivre une multiplication sexuée dans les cellules de la muqueuse intestinale (petit intestin) et par la suite seront excrétés sous forme d’oocystes dans les matières fécales.

Hote intérmédiaire: mammifères et oiseaux hébergent des parasites
dans leurs tissus (kystes contenant des bradyzoïtes). Contamination de hote intermédiaire se fait par l’ingestion des kystes tissulaires ou l’ingestion d’oocystes. Les sporozoïtes libérés par les oocystes ou les bradyzoïtes libérés des kystes entrent dans les cellules de la muqueuse intestinale où ils se transforment en tachyzoïtes (forme mutliplicative intracellulaire) ensuite il y a libération de tachyzoïtes par les cellules infectées, dissémination sanguine pour infecter d’autres cellules dans différents organes. Lorsque la réponse immunitaire se dévéloppe, les tachyzoïtes se transforment en bradyzoïtes, formes latentes intracellulaires (résistantes aux facteurs environnementaux) qui forment des kystes surtout dans muscles et tissus nerveux (SNC)
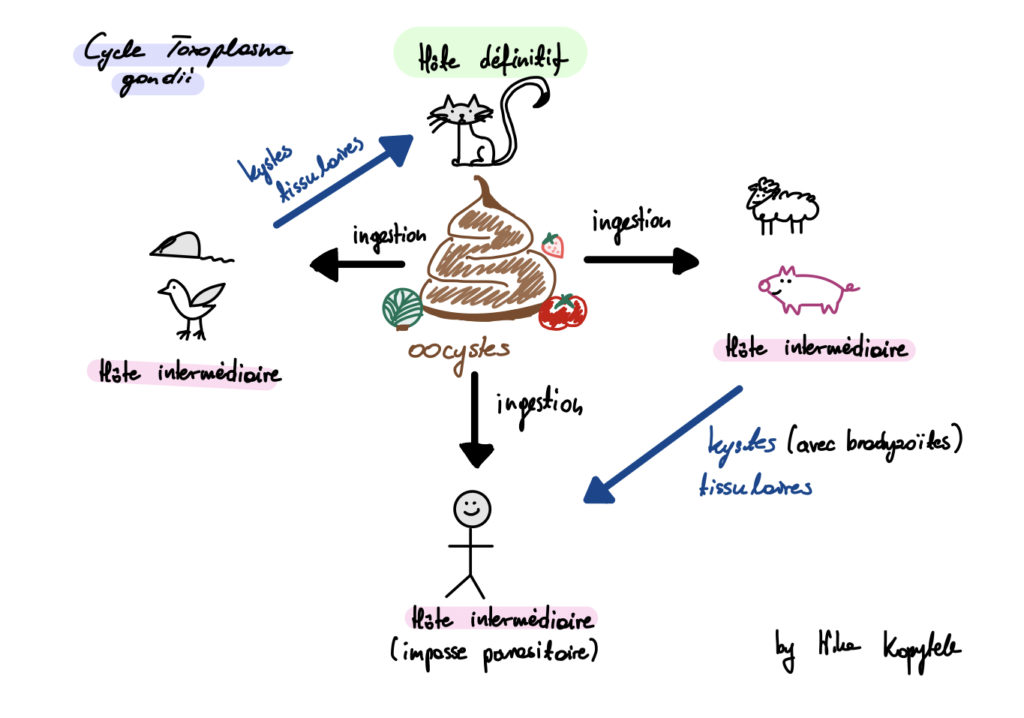
- Les kystes persistent à vie dans les tissus de l’hôte infecté
- On peut observer la réactivation et multiplication en cas d’immunodéficience
On différencie 2 phases dans le développement de l’infection: phase aigue et phase chronique.
- Phase aigue: les symptômes seront lié à la destruction des cellules infectées ce qui résulte de la réaction inflammatoire allants meme au stade de nécrose. C’est qui explique qu’on peut retrouver des fois les calcifications dans les tissus.
- Phase chronique: qui est une phase asymptomatiques, lié à la persistance des kystes à bradyzoites.
- Quels organes seront atteints?
Alors, il n’y a pas un endroit spécifique qui serait atteint. Il faut savoir que tous les tissus peuvent être potentiellement touchés: foie, tissu lymphoïde, poumons, muscles, système nerveux central, rétine, d’où importance d’y penser si on suspect infection symptomatique à toxoplasmose.
Transmission
De l’animal à l’homme: voie orale
- Via mains souillées (litière chats, jardinage, chatons ayant des oocystes matures sur le pelage)
- ingestion de légumes crus contaminés
Forme infectante la + efficace (stade le + résistant au pH intestinal) - ingestion de viande crue ou insuffisamment cuite provenant d’un animal infecté
Interhumaine: transmission congénital in utéro
Syndrome
L’infection à toxoplasmose est majoritairement asymptomatique ce qui explique sa grande prévalence (30% mondiale). Ce qu’il faut souligner c’est que le fait de s’infecter ne veut pas absolument dire qu’on va developper la maladie (prévalence 10%).Présentation clinique est strictement lié à la phase de cycle donc respectivement phase aigue et chronique (asymptomatique).
Infection aigue symptomatiques:
- Toxoplasmose ganglionnaire bénigne: 10% des personnes infectés, se présente sous la forme de triade symptomatique: fievre, adénopathies (surtout cervicales, chaîne moyenne ou postérieure, ganglions mobiles, peu douloureuses), asthénie (de long durée). Bonne nouvelle, l’evolution est favorable spontanée.
- toxoplasmose occulaire: provoque uvéite postérieure, rétinite ou choriorétinite; foyers toxoplamsqiue sont blancs, cotonneux et peu hémorragiques.
- toxoplamsose grave des immunodéprimés: dans le cas de l’infection acquise (transplantation) ou réactivation de kystes (chez des patients préalablement infectés). C’est une infection opportuniste parasitaire la plus fréquente chez les immunodéprimés On distingue principalement 3 formes: encephalitis use, pulmonaire, oculaire.
- toxoplasmose congénitale:
- Avortement ou mort périnatale
Formes symptomatiques: pouvant provoquer décès dans les premiers mois ou retard psychomoteur et/ou troubles de la vision irréversibles.
- Toxoplasmose encéphalitique: hydrocéphalie
- syndorme neurolgoique ou souffrance cérébrale se présentant sous forme des: convulsions, hyper ou hypotonie, altérations des reflexes, troubles végétatifs
- toxoplasmose oculaire sous forme de chorio-rétinite
Si asymptomatique à la naissance, dans 85-90% des cas sans traitement on peut observer séquelles oculaires ou retard mental.
Diagnostic
1. Toxoplasmose ganglionnaire bénigne:
- Prise de sang qui montrera syndrome mononucléosique (inconstant), caractérisé par leucocytose modérée avec lymphocytoss et neutropénie relative, légère augmentation des éosinophiles sanguins. C’est important dans ce cas de faire diagnostic différentiel avec EBV et CMV.
- Diagnostic immunologique: est un moyen de diagnostic fondamental dans ce cas avec seuil des anticorps 10 UI/ml. Techniques utilisés sont suivantes:
Dye-test de Sabin et Feldman (trust de référence OMS). Principe est de mettre les parasites vivantes en présence de serum de patient et détecter s’il y’a ou pas lyse des parasites ce qui confirmera l’existance des anticorps dans le sérum.
Agglutination directe: dans le cas positive on va voir agglutination entre les anticorps et les parasites
Immunofluorescnce indirecte et ELISA: Enzyme-linked-immunosorbent-assay: dans les deux cas si le test est positif on verra illumination du à la réaction entre des anticorps dirigés contre les anticorps anti-Toxoplasmosa
Hemagglutination indirecte: détection des anticorps par agglutination avec les hématites possédants l’antigène sur leur surface.
2. Toxoplasmose oculaire
- fond d’œil
3. Toxoplasmose d’immunodéprimés
- Scanner cérébral avec contraste: on va voir l’images hyperfixantes annulaire ou nodulaire ce qui traduit l’œdème autour de centre hypodense.
- IRM cérébral: si scanner est négatif et la suspicion clinique est forte. Ici on verra multiples petites lésions.
- diagsnotic parasitologique par observation directe des tachyzoites sur les prélèvements sur frottis de sang, LCR, LBA ou par l’observation sur la culture sur lignée cellulaire, incubation à la souris ou dans les cas extrêmes, sur la biopsie cérébrale.
- Diagnostic par technique PCR sur les prélèvements comme sang, LCR
- Diagnostic Immunolgoique peut contributif (contrairement à la forme ganglionnaire bénigne ou on utilise surtout techniques immunologiques et PCR n’est pas contributif)
4. Toxoplasmose congénitale
- Imagerie médicale: sur échographie, fœtale et néonatale on peut voir dilatation des ventricules cérébraux . Sur radiographie et scanner crânien on verra des lésions pathognomoniques pour toxoplasmose tel que calcifications intra-crâniennes dans le slopes cérébraux ou péri-ventriculaires.
- diagnostic biologique
Prénatal sur liquide amniotique on recherchera ADN parasitaire, les anticorps IgM et IgA et éventuellement parasites vivants par les techniques: PCR, ISAGA et microscopie optique, respecitvement.
Néonatal: sur le sang de cordon ombilical on recherchera le meme chose que dans le diagnsotic prénatal et en plus on pourra détecter les IgG par la technique de Westernblot et la réponse immunitaire cellulaire via technique de IGRA.
Postnatal: sur le prélèvement de sang périphérique on rechercha la meme chose qu’en période néonatale et en plus IgG anti-toxoplasma à 10-12 mois via technique d’ELISA.
- Dans le cas de suspicion de primo-infection chez le bébé il faut pas oublier de suivre cliniquement l ‘enfant dans le cadre des lésions cérébrales et oculaires. L’écartement définitif de diagnostic congénital par confirmation d’absence des anticorps spécifiques d’isotope IgG est possible que à l’âge de 1 an. Sinon jusqu’à 1 an on va continuer suivi sérologique pour éventuelle détection des IgG.
Techniques de diagnsotic biologique dans le cas de suspicion de l’infection congénitale à toxoplasmose
- IgM et IgA: on va commencer par immunocapture via ISAGA qui permettra d’isoler IgM et IgA et d’éviter les tests faussement positifs dûs à la compétition entre les anticorps IgG et IgM et IgA et par la suite on mettra les anticorps isolés en contact avec les parasites pour observer (résultat positif) ou pas (résultat négatif) la sédimentation des parasites colorés.
- IGRA: mise en solution de sang total de cordon ombilicale ou périphérique avec lysat de Toxoplasma et par la suite mise en évidence de la production de IFN-gamma dans le surgeant par les lymphocytes T.
- Westernblott nous permet de comparer le sang du bébé avec le sang de la mere pour observer éventuellement les IgG absents chez la mere et présents chez l’enfant témoignant infection congénitale chez l’enfant. Attention si les deux échenillions sont identique le test est non concluant donc on n ne peut pas confirmer absence ou présence de primo-infection chez l’enfant.
Prévention
1. Toxoplasmose ganglionnaire bénigne: inutile en dehors de la gestation parce que comme on a déjà mentionnés, la plupart des infections sont asymptomatiques. Sinon on peut inactiver les kystes par congélation de la viande (-7°C pendant 4 jours) ou par la chaleur (min 58°C pendant 15 minutes) ou par irradiation. Pour inactiver les locustes sur la fruits et légumes on aura besoin de congélation à -20°C pendant 3 semaines ou chauffage à 58°C pendant 15 minutes. Il faut souligner que les désinfectants n’ont pas d’effet sur la prévention de l’infection.
2. Toxoplasmose occulaire: il n’existe pas de prévention spécifique pour cette forme de toxoplasmose.
3. Toxoplasmose d’immunodeprimé: on peut prévénir ou limiter la réactivation de l’infection par administration de cotrimoxazole ou l’association de dapsone avec pyrmiéthamine
4. Toxoplasmose congénitale: Vu la gravité des conséquences de primo-infection congénital, la prévention est primordial. Malgré les techniques diagsnotic unes poussées on ne peut pas malheureusement détecter tous le infeciton à temps d’où importance d’identifier les femmes à risuqe de transmission congénitale. Les paremetres suivis sont: taux IgM et IgG, evolution des taux de Ac dans le temps, avidité IgG (augmente avec durée d’infection). Dans l’idéal on devrait connaître statut immunitaire de la femme avant qu’elle tombe enceinte, malheureusement cela n’est pas toujours le cas donc on va plutôt essayer de suivre leur statut pendant le grosses pour détecter précocement l’apparition des IgM ou IgG.
Intérperation des résultats de la sérologie maternelle:
- Absence IgG et IgM: cela signifie que la mere n’a pas été infecté préalablement donc elle est bine à risque de developper primo-infection et la transmettre au bébé. On confirme les résultats dans 15j- jours qui suivent et on informe la femme sur la prevention primaire qui consiste à application de mesures afin d’éviter l’acquisition de l’infection pendnat la grossesse.
- Appariton des IgG: on confirme le résultat dans 15 jours qui suivent et on rassure la femme vu qu’elle a déjà eu l’infection aigue et elle est passé au stade chronique, à priori il n’y a pas de risque de primo-infection pour l’enfant.
- Présence des IgG > IgM: il faut confirmer la stabilité des IgM par deux même prélèvement dans 15 jours qui suivent ce qui nous permettra de confirmer que l’infection est ancienne et donc assurer la femme qu’il n’a pas, à priori, le risque pour son futur bébé.
- Présence IgM>IgG: malheureusement cela signifie l’infection débutante donc en fonction de trimestre le risque de mortalité et des séquelles sera plus ou moins élevé. On va proposer prophylaxie secondaire qui consiste à rechercher l’infection fœtale, soit traitement, soit IVG.
Prévention primaire: permet d’éviter 90% des primo-infection maternelles
- Ne pas manger de la viande crue ou peu cuite
- lavage des mains apres anipualation de viande crue ou contact avec les chats
- port des gants pour travail dans le jardin
- pas toucher literie du chat
Prophylaxie secondaire: permet diminuer la morbidité fœtale de 70%. On va traiter l’infection maternelle pour limiter les séquelles chez l’enfant et suivi sérologique de l’enfant. Le traitement est une association de pyriméthamine et sulfadiazine à partir de 18ème semaine de la grossesse. On va continuer la thérapie jusqu’à l’accouchement.
Traitement
- Toxoplasmose ganglionnaire bénigne: spiramycine pendnat 3-4 semaines. Attention ce traiatemtn est actif uniquement sur la tachyzoites donc pas sur les bradyzoites intra-kystiques.
- Toxoplasmose oculaire: Pyriméthamine et la Sulfadiazine.
3. Toxoplasmose chez immunideprimés: association de pyriméthamine et sulfadiazine ou clindamycine per os pendant 6 semaines. Dans le cas d’œdème cérébrale on peut appliquer les anti-convulsivants et corticothérapie.
4. Toxoplasmose congénital: dans le cas confirmé par la présence des IgG anti-Toxoplasma on va traiter l’enfant pendant au moins un an par: Pyrimethamine 1mg/kg/j per os en associai ont en sulfadiazine 50-100 mg/kg/j en 2 doses per os. Il faut pas oublier d’ajouter acide folique. Malheureusement le traitement a un effet limité sur l’apparition des lésions oculaires à long terme.
Remarque
- Il y a quelques années les chercheurs ont étudié l’effet de la toxoplasmose sur les comportements des rongeurs qui a montré chez les rats en phase chronique disparition des comportements d’adaptation à la survie (les rongeurs ne ressentaient pas peur des urines des chats et même ils semblaient d’être attiré par celle-ci).
- Il y a des études qui mettent l’infection à toxoplasmose en lien avec les troubles psychiatriques comme dépression et schizophrénie.
- Le taux de transmission in utero est le plus élevé dans premier trimestre et puis diminue progressivement. Ce qui veut dire que la proportion des nouveaux-nés présentant des symptômes à la naissance et mortalité sera plus élevé au début de la grossesse et diminuera progressivement réduisant la mortalité de 5% jusqu’à 0%. Par contre le risque des séquelles à la naissance et à long term sera non-négligeable pendant toute la durée de la grossesse.
